L'Agence européenne des médicaments approuve le vaccin Moderna, "sûr et efficace"
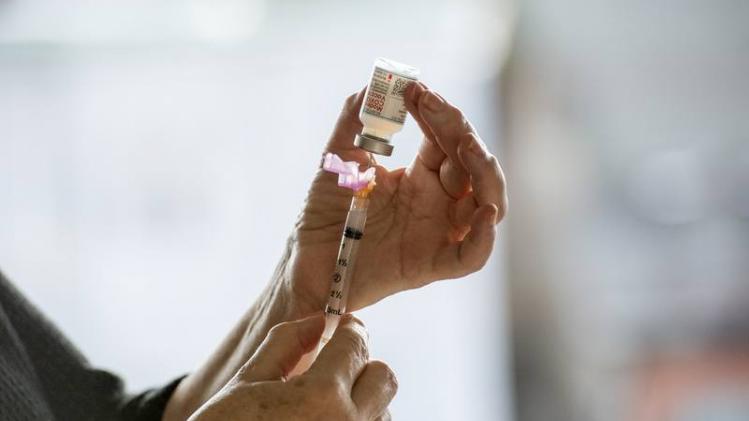
Si la Commission européenne donne également son feu vert, ce vaccin contre le virus SARS-CoV-2 deviendra le deuxième accessible sur le marché européen, après celui de BioNTech/Pfizer le 21 décembre dernier.
Un vaccin "sûr et efficace"
"L'Agence européenne des médicaments (EMA) a jugé le vaccin de Moderna sûr et efficace. C'est une bonne nouvelle pour nos efforts visant à fournir davantage de vaccins aux Européens", a commenté la présidente de la Commission, Ursula von der Leyen. Elle a assuré que l'exécutif européen œuvrait maintenant "à pleine vitesse" afin de délivrer son approbation. Une première réunion de l'EMA lundi n'avait pas permis d'aboutir, plusieurs questions posées par les Etats membres restant en suspens.
Un vaccin en deux doses
Les Etats-Unis, le Canada et Israël avaient déjà validé le vaccin, accroissant de facto la pression sur l'UE, où les demandes d'accélération de la vaccination se multiplient. L'Union a réservé 160 millions de doses du vaccin Moderna. Leur répartition entre les 27 Etats membres doit être proportionnelle à la population. Ce vaccin se prend en deux doses, à quelques semaines d'intervalle, comme celui de Pfizer/BioNTech. Mais la formule de Moderna peut être conservée à -20°C, et non -70°C comme pour le remède de Pfizer, qui a forcé le groupe à développer des containers spécifiques pour le transport.